1.5小鼠肝、脾定殖能力测定
将鼠伤寒沙门菌标准菌株LT2及基因缺失菌株ΔompN、ΔfadL、ΔybfM、Δhfq、ΔrybB、ΔrybB&Δhfq菌液浓度调整为1×108CFU·mL-1,制备方法同1.4.将小鼠随机分组,每组5只,腹腔注射菌液0.5 mL·只-1,分别在6和48 h后取小鼠肝脏和脾脏称重,计算肝脏、脾脏指数.匀浆后使用无菌PBS稀释,取100μL稀释液进行10和100倍稀释涂板,重复3次,置于37℃温箱中过夜培养,菌落计数,计算相应组织的载菌量.
1.6数据处理
数据以平均值±标准偏差表示,通过GraphPad Prism 8.0.2软件分析数据和制图.
2结果与分析
2.1鼠伤寒沙门菌株生长曲线
由图1可以看出:鼠伤寒沙门菌标准菌株LT2及基因缺失菌株ΔompN、ΔfadL、ΔybfM、Δhfq在液体LB中有相似的生长曲线;虽然ΔrybB和ΔrybB&Δhfq生长速度相较于标准菌株有所减缓,但是变化不显著.
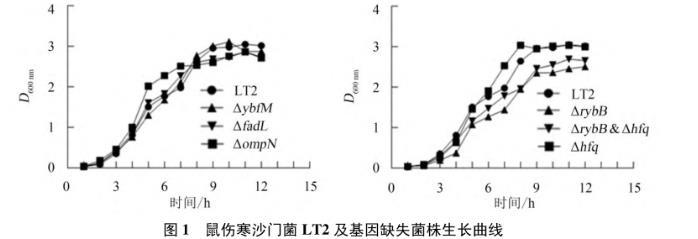
图1鼠伤寒沙门菌LT2及基因缺失菌株生长曲线
2.2鼠伤寒沙门菌株的毒力
结果显示:鼠伤寒沙门菌标准菌株LT2对小鼠的LD50为3.97×107CFU;基因缺失菌株ΔompN、ΔfadL、ΔybfM对小鼠的LD50分别为1.58×105、6.29×105、9.97×105CFU,与LT2相比毒力明显增强;基因缺失菌株Δhfq和ΔrybB&Δhfq对小鼠的致死率未高于50%;而基因缺失菌株ΔrybB对小鼠的LD50为9.97×107CFU,与LT2相比毒力有所下降(表2).
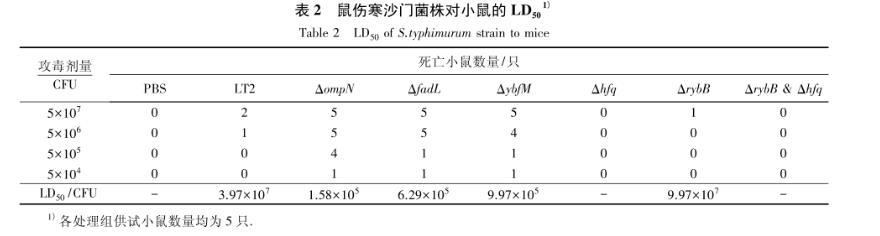
表2鼠伤寒沙门菌株对小鼠的LD501)
2.3基因缺失菌株在脾脏上的定殖能力
图2显示:小鼠腹腔注射各菌株6 h后,相对于LT2,Δhfq、ΔrybB、ΔfadL、ΔybfM处理组的脾脏指数极显著上升(P<0.01);ΔrybB&Δhfq处理组的脾脏指数显著上升(P<0.05);而ΔompN处理组的脾脏指数低于LT2,但差异不显著(P>0.05).图3显示:相对于LT2,小鼠注射Δhfq6 h后脾脏上的载菌量显著降低(P<0.05);注射其余菌株后的脾脏载菌量与LT2差异不显著(P>0.05).
小鼠注射各菌株48 h后,相对于LT2,各处理组的脾脏指数极显著升高(P<0.01)(图2).相较于LT2,注射ΔrybB&Δhfq和Δhfq48 h后脾脏上的载菌量显著降低(P<0.05);注射其余菌株后脾脏上的载菌量与LT2差异不显著(P>0.05)(图3).
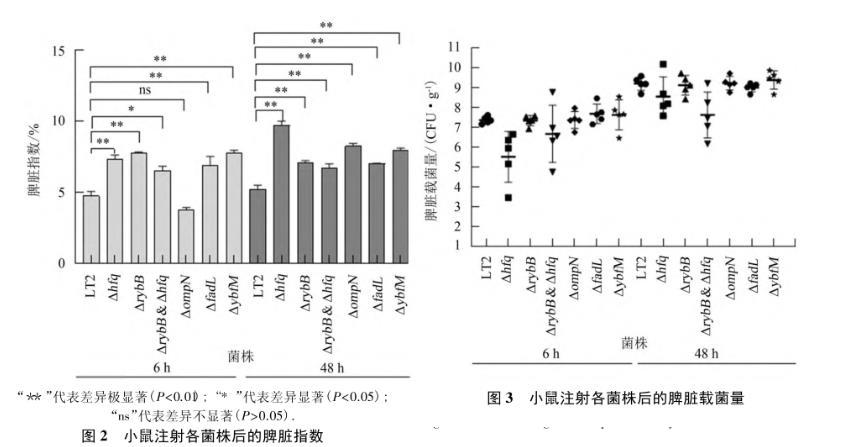
“**”代表差异极显著(P<0.01);“*”代表差异显著(P<0.05);“ns”代表差异不显著(P>0.05).图2小鼠注射各菌株后的脾脏指数
2.4基因缺失菌株在肝脏上的定殖能力
图4显示:小鼠腹腔注射各菌株6 h后,相对于LT2,Δhfq、ΔrybB&Δhfq、ΔompN处理组的肝脏指数极显著下降(P<0.01);ΔybfM处理组的肝脏指数显著下降(P<0.05);而ΔrybB和ΔfadL处理组的肝脏指数变化不显著(P>0.05).图5显示:相对于LT2,小鼠注射Δhfq和ΔrybB&Δhfq6 h后的肝脏载菌量显著降低(P<0.05);而ΔompN、ΔfadL、ΔybfM、ΔrybB处理组的肝脏载菌量无显著变化(P>0.05).
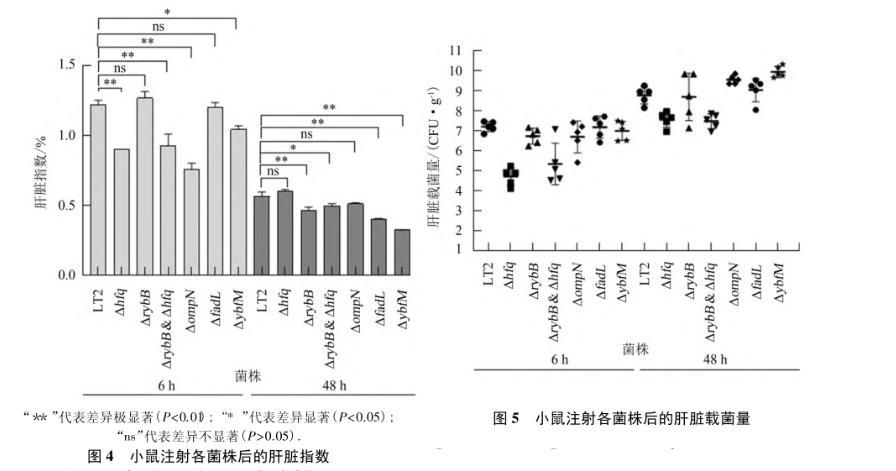
“**”代表差异极显著(P<0.01);“*”代表差异显著(P<0.05);“ns”代表差异不显著(P>0.05).图4小鼠注射各菌株后的肝脏指数Fig.4 Liver index of mice after injected with different strains
小鼠注射各菌株48 h后,相对于LT2,ΔrybB、ΔfadL、ΔybfM处理组的肝脏指数极显著下降(P<0.01);ΔrybB&Δhfq处理组的肝脏指数显著下降(P<0.05);而Δhfq和ΔompN处理组的肝脏指数变化不显著(P>0.05)(图4).相对于LT2,注射ΔrybB和ΔfadL48 h后肝脏载菌量变化不显著(P>0.05);而Δhfq和ΔrybB&Δhfq处理组的肝脏载菌量显著下降(P<0.05);ΔompN和ΔybfM处理组的肝脏载菌量显著上升(P<0.05).
