肠道微生物群的失调与代谢综合征(MetS)的发病机制有关,并且肠道微生物可能通过产生的有害代谢物损害宿主新陈代谢。
2024年7月19日,复旦大学生命科学学院于肖飞、上海交通大学医学院附属仁济医院陈磊及耶鲁大学医学院Marc Schneeberger等人在Nature子刊Nature Metabolism上发表了题为:Hydrogen sulfide produced by the gut microbiota impairs host metabolism via reducing GLP-1 levels in male mice的研究论文。
该研究表明,在代谢综合征(MetS)患者中富集的肠道共生菌脱硫弧菌(Desulfovibrio),通过产生硫化氢(H₂S)抑制肠道激素胰高血糖素样肽-1(GLP-1)的产生,进而破坏宿主代谢,而阻断脱硫弧菌和硫化氢的产生,可提高GLP-1的产生,并改善饮食诱导的代谢紊乱和肥胖。这项研究揭示了肠道微生物影响代谢健康的新机制。
肠道微生物群对宿主生理有着关键且深远的影响,长期以来,其一直与多种代谢综合征有关,包括肥胖、2型糖尿病和心血管疾病等。之前的研究已经发现了肠道微生物产生的有害代谢产物(例如三甲胺)会进入宿主循环并直接靶向内脏器官参与代谢综合征的发病。但许多肠道微生物的代谢物无法进入宿主循环,可能通过中继途径影响宿主。
肠内分泌细胞(EEC)是分散在整个肠道上皮的化学感应细胞,与肠道微生物群及其代谢产物在空间上接近。EEC能够感知肠道腔内存在的营养信息,并分泌激素来协调远端器官的代谢过程。例如,肠内分泌L细胞在食物摄入后产生关键的代谢激素胰高血糖素样肽-1(GLP-1),它刺激胰腺β细胞产生胰岛素,减缓胃肠蠕动,并抑制大脑中的食欲,以通过肠道激素介导的信号传递来维持代谢平衡。事实上,在饮食诱导的肥胖(DIO)小鼠和患有代谢综合征(MetS)的患者中,已有研究观察到了GLP-1生成的缺陷。相反,GLP-1产生增加与高纤维饮食的代谢益处相关,而GLP-1信号通路的药理激活提供了前所未有的临床意义,包括治疗2型糖尿病、减肥等。
肠内分泌细胞(EEC)处于理想位置,可启动并传递肠道微生物群-宿主相互作用,其能被微生物代谢产物(例如短链脂肪酸和次级胆汁酸)所刺激。然而,关于肠内分泌细胞在代谢综合征中是否会受到有害微生物代谢产物的靶向作用,我们仍知之甚少。
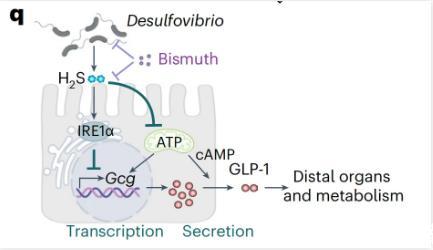
在这项最新研究中,研究团队发现,代谢综合征(MetS)所富集的肠道共生菌脱硫弧菌属(Desulfovibrio spp.)通过其特征性代谢产物硫化氢(H₂S)抑制肠内分泌L细胞的线粒体呼吸并诱导非折叠蛋白反应,从而抑制的产生和分泌,进而损害宿主的代谢健康。
值得注意的是,用一种非处方药碱式水杨酸铋来阻断脱硫弧菌和硫化氢(H₂S),可提高GLP-1的产生,并改善雄性小鼠饮食诱导的代谢紊乱和肥胖。
这项研究揭示了脱硫弧菌代谢产物硫化氢(H₂S)损害了GLP-1的产生,阐明了肠道微生物有害代谢产物在代谢综合征(MetS)中损害宿主代谢的肠道相关机制,并为治疗代谢综合征提供了新的可能性。
相关新闻推荐
3、大肠杆菌中Tat标签融合蛋白的高表达机理探究:基于mRNA转录与蛋白质二级结构的分析
