2.2 hrcN基因打靶序列片段的构建
突变体筛选的抗性基因采用Gm抗性基因(长度832 bp),hrcN基因上游同源重组臂和下游同源重组臂长度分别为799和742 bp,利用融合PCR技术构建打靶序列片段(上游同源重组臂-Gm抗性基因编码序列-下游同源重组臂),长度为2373 bp。图3电泳图显示,泳道1中有4条带,其中最亮的条带为打靶序列片段,电泳结果表明成功构建了打靶序列片段。

2.3 hrcN基因突变株的构建
将供菌体和受菌体(CBM613菌株)混合结合后,抗性平板上培养单克隆,随机挑选10个单克隆,用hrcN基因内部引物进行PCR鉴定。如发生二次重组,则这对引物无扩增产物,否则有227 bp的特异性扩增条带。图4结果显示:第1~6号克隆为阴性扩增,表明hrcN基因可能已被敲除;7~10号克隆有227 bp的特异性条带,说明没有发生二次重组,hrcN基因未能成功敲除。
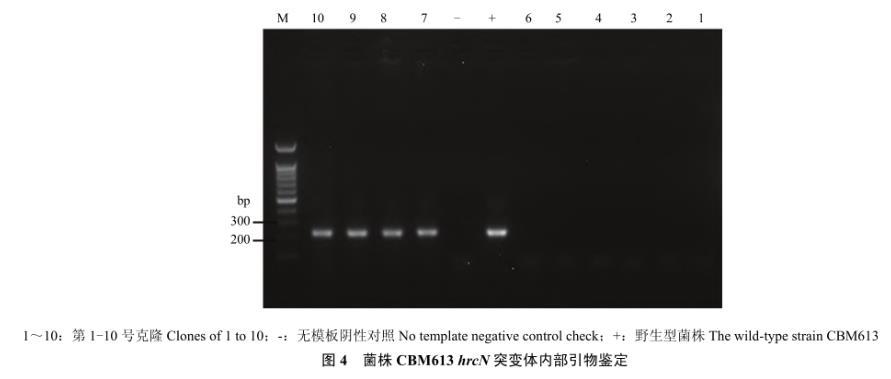
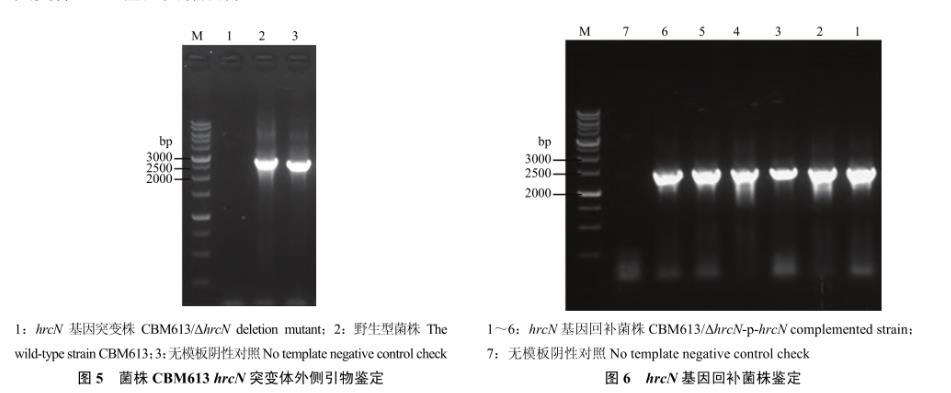
将上述1号克隆再次进行hrcN基因内部引物鉴定,为阴性扩增后用hrcN基因外侧引物进行进一步的鉴定。图5显示,条带2为原始菌株的扩增产物长度为2739 bp;条带1为Gm抗性基因替换菌株的扩增产物长度为2580 bp,同时测序结果显示局部序列同设计。该克隆子为最终的hrcN基因被Gm抗性基因替换的阳性克隆,称为:CBM613/ΔhrcN。
2.4回补菌株的筛选及鉴定
在Tc平板上的阳性克隆用pRK415-F/pRK415-R载体引物对进行PCR鉴定。当hrcN克隆入设计位点后,这对引物的扩增产物长度为1634 bp。图6结果显示,1~6号全部克隆都有预期长度的特异片段扩增,取第1号克隆的PCR产物进行测序,结果显示与设计一致。经转化CBM613/ΔhrcN受体菌后,涂布筛选出阳性克隆,pRK415-F/pRK415-R引物进行PCR扩增,有预期长度的特异片段扩增,表明青枯雷尔氏菌突变株hrcN基因回补成功。
2.5 hrcN基因对青枯雷尔氏菌致病力的影响
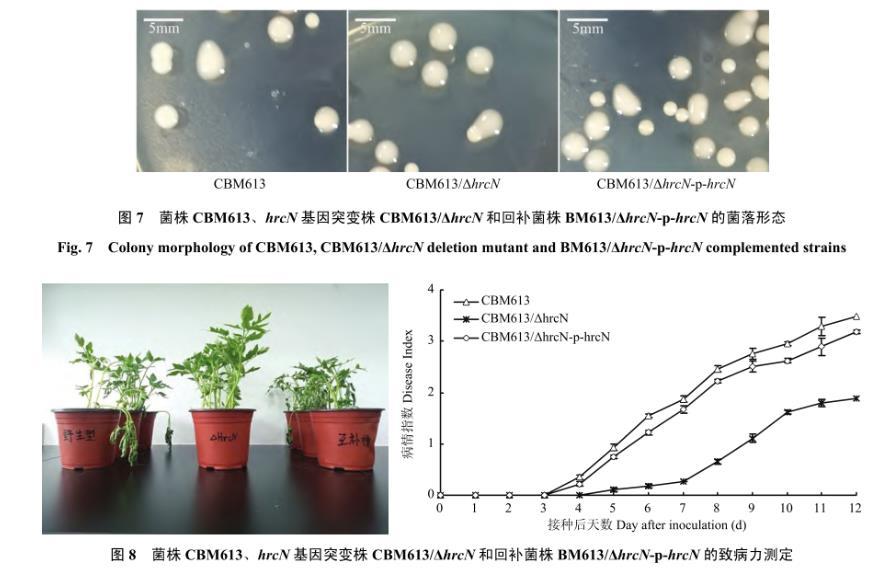
hrcN基因敲除后,在NA培养基上28℃生长5 d,突变株和回补菌株菌落形态与野生型菌株相比无明显变化(图7)。进一步将野生型菌株、hrcN基因突变株和回补菌株采用根部接种法接种番茄测定致病力结果表明,野生型菌株接种番茄植株后,在第4 d开始发病,突变株在第5 d才开始出现萎蔫症状。图8为野生型菌株、突变株和回补菌株在接种后第7 d的发病情况可知,野生型菌株的病情指数为1.87,突变株仅为0.27,下降了85.56%;相比野生型菌株,回补菌株病情指数为1.67,突变株的致病力能够部分恢复。接种12 d后,野生型菌株的病情指数高达3.49,而突变株仅为1.89,回补菌株有所恢复为3.18。接种试验结果显示:突变株较野生型菌株的致病力下降,病程延长,但并未丧失致病力,表明hrcN基因是青枯雷尔氏菌致病性相关的重要基因。
2.6 hrcN基因对青枯雷尔氏菌生长曲线的影响
分别将CBM613菌株、CBM613/ΔhrcN突变株和CBM613/ΔhrcN-p-hrcN回补菌株在Boucher基础液体培养基(贫营养培养基)和CPG培养基(富营养培养基)中进行生长曲线测定,野生型菌株、突变株和回补菌株在富营养培养基上的生长速率差异不明显(图9)。

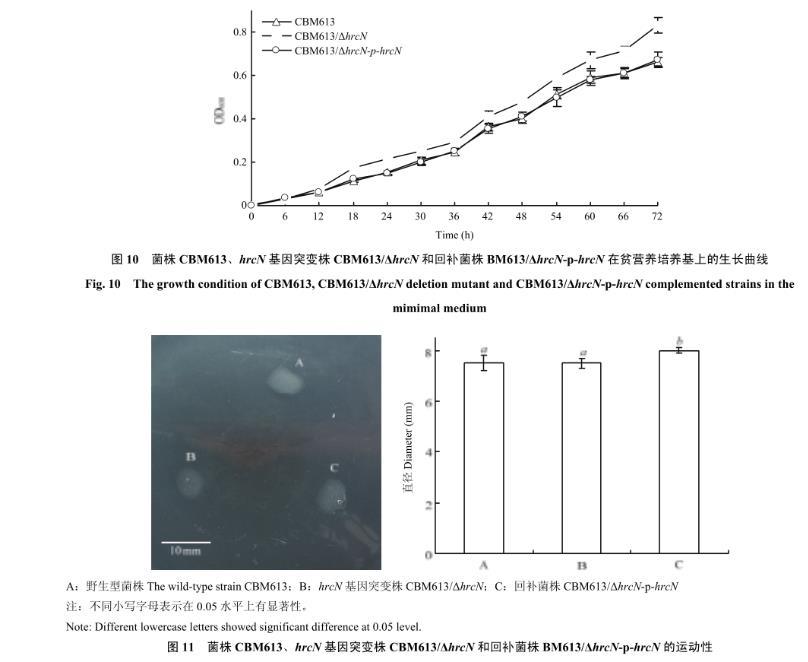
3种青枯雷尔氏菌在贫营养培养基上培养18 h后,突变株比野生型菌株生长更快(图10),生长速率开始出现明显差异(P<0.05),回补菌株与野生型菌株生长速率无明显差异。
2.7 hrcN基因对青枯雷尔氏菌运动性的影响
利用半固体SMM培养基,研究CBM613菌株、CBM613/ΔhrcN突变株和CBM613/ΔhrcN-p-hrcN回补菌株的运动性。通过测量菌落直径,野生型菌株、突变株和回补菌株的运动能力没有显著差异,结果表明hrcN基因敲除没有影响青枯雷尔氏菌的运动性(图11)。
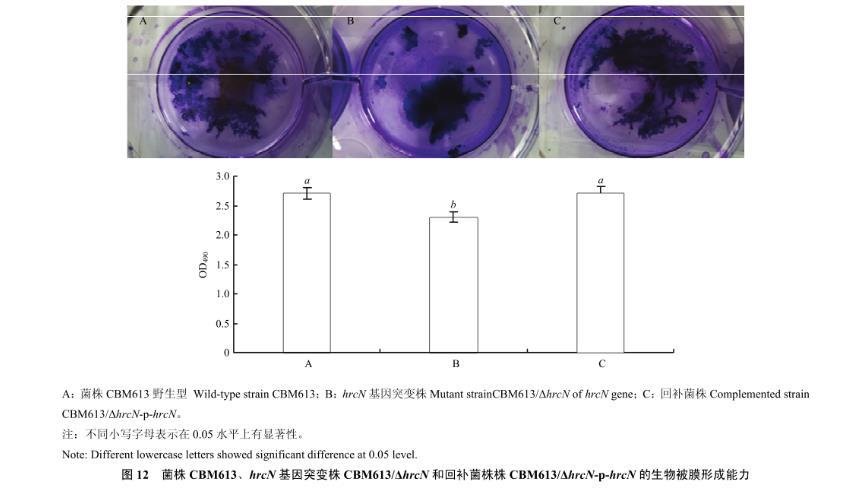
2.8 hrcN基因对青枯雷尔氏菌生物被膜形成能力的影响
通过对比菌株CBM613、CBM613/ΔhrcN突变株和CBM613/ΔhrcN-p-hrcN回补菌株的生物被膜形成能力,结果发现3种青枯雷尔氏菌株的生物被膜形成能力随培养时间增加而增强,突变株相比于野生型菌株,生物被膜形成能力显著减弱,而回补菌株与野生型菌株相比差异不明显(图12)。
相关新闻推荐
1、肠膜明串珠菌肠膜亚种LA-07生长曲线制作和世代时间计算
2、Act0988放线菌拮抗菌株的鉴定、培养条件与菌株生长关系、发酵工艺(一)
