2结果与分析
2.1菌体生长及产酶曲线
对菌体进行摇瓶发酵,每2 h取少量发酵液测其酶活力和在600 nm处的吸光值,由图1知,发酵前期菌体生长速度较快,在20 h后生物量基本达到平衡,酶活力在24~26 h处达到最大。
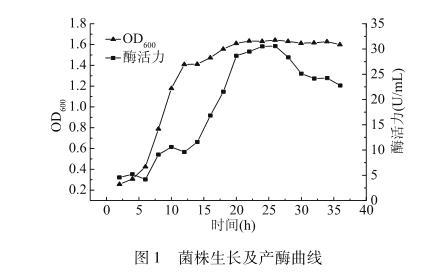
图1菌株生长及产酶曲线
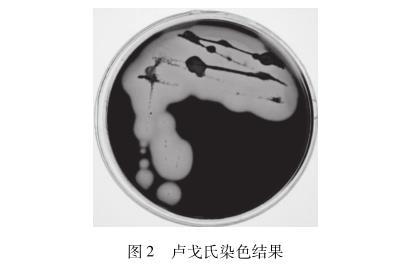
图2卢戈氏染色结果
2.2筛选及形态学鉴定
将该菌在平板上培养24 h后,培养基表面形成明显白色菌落,菌落表面湿滑,边缘平整,中央凹陷。对菌落进行卢戈氏碘液染色,染色结果如图2所示,菌落周围形成明显的透明水解圈,这是由于培养基被降解的部分生成具有还原性的寡糖,不能被卢戈氏碘液染色,而未被降解掉的部分能够被卢戈氏碘液染成深色。对菌落进行革兰氏染色镜检结果如图3所示,菌体被染成红色,表明该菌属革兰氏阴性菌,与已报道的绝大多数产琼胶酶菌株属革兰氏阴性菌结果相符。

图3革兰氏染色镜检结果
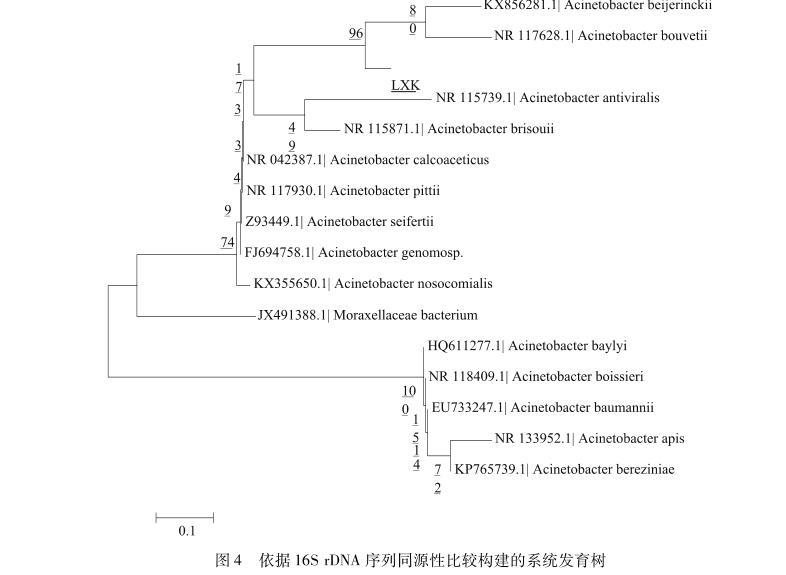
图4依据16S rDNA序列同源性比较构建的系统发育树
2.3系统发育树的构建
用MEGA6.0软件,根据16S rDNA序列相似性,将该菌与NCBI数据库中相应的细菌一起构建系统发育树,由系统发育树可知,该序列与Acinetobacterbeijerinckii(Genbank Accession No.KX856281.1)和Acinetobacterbouvetii(Genbank Accession No.NR117628.1)等菌属相似性高达99%,能够证明菌LXK为不动杆菌(Acinetobactersp.)。目前,不动杆菌产琼胶酶的研究报道较少,仅Lakshmikanth等人和陈虹等人从土壤中筛选出能够产琼胶酶的不动杆菌,从海洋环境中分离出产琼胶酶的不动杆菌未见报道。
2.4酶解反应最适温度的确定
将酶反应体系分别置于20、30、40、50、60和70℃的水浴中反应,测定各温度下琼胶酶活力,结果见图5。从图5中可以看出,最适酶解温度为40℃,温度过高和过低都不利于酶解,这与来自不动杆菌AG LSL-1、紫色杆菌SY12、弧菌JMUAZ6的琼胶酶的最适酶解温度相同。由于琼胶具有凝固性,当温度较低时底物发生凝固,粗酶液与底物的接触面积减少,酶解效率降低;温度过高时,酶受热失活,同样影响酶解效率。
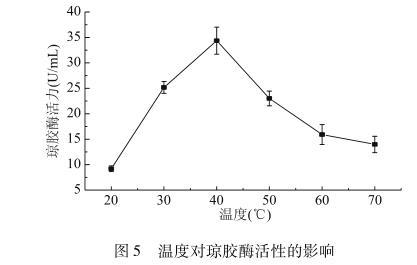
图5温度对琼胶酶活性的影响
2.5酶解反应最适底物浓度的确定
选取0.1%~1.0%的浓度梯度研究琼脂粉浓度对琼胶酶活力的影响,实验结果见图6。从图6中可以看出,随着底物浓度的增大,琼胶酶活力随之增大,在底物浓度为0.5%时琼胶酶活力达到最大值,继续增大底物浓度,琼胶酶活力逐渐下降,原因是底物浓度过大,降低了分子的扩散性,降低酶解反应效率。因此,酶的最适底物浓度为0.5%。
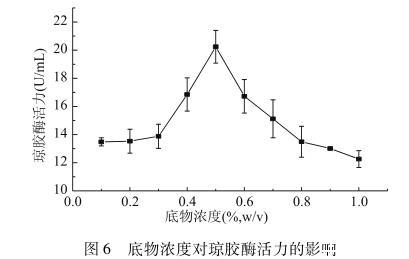
图6底物浓度对琼胶酶活力的影响
2.6酶解反应体系最适pH的确定
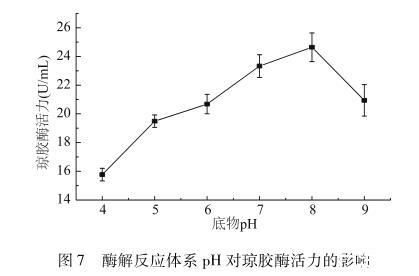
图7酶解反应体系pH对琼胶酶活力的影响
反应体系pH可以影响酶的结构和稳定性,同时底物和酶的解离状态也受pH的影响。为探究反应体系pH对琼胶酶活力的影响,选取pH4.0~9.0六个pH梯度进行酶解实验,结果见图7。由图7可知,琼胶酶活力随着体系pH的增大呈现先增大后减小趋势,在pH8.0附近达到最大值,继续增大pH,琼胶酶活力反而下降,可能是强碱性环境导致酶蛋白变性从而使琼胶酶失活。
2.7金属离子对酶解反应的影响
选取7种金属离子研究它们对酶解反应的影响,结果见图8。从图中可以看出,K+和Ca2+能促进酶解反应,Na+和Mg2+对酶解反应的影响较小,而Fe2+、Mn+和Ba2+对酶解反应起抑制作用,此结果与琼胶酶降解菌Agarivoranssp.LQ48、Vibriosp.JMUAZ5研究结果相似。
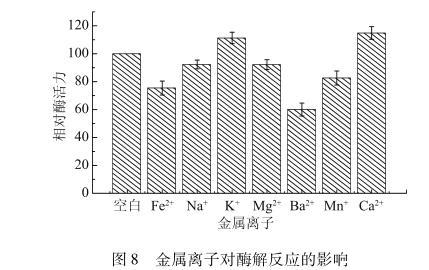
图8金属离子对酶解反应的影响
3结论
本研究通过大量筛选工作,从海洋环境分离得到一株具有琼胶酶活性的细菌,通过镜检发现该菌为革兰氏阴性菌,并通过16Sr RNA基因序列的测定,确定该菌为不动杆菌,是首次从海洋环境中分离出的能够产琼胶酶的不动杆菌,并命名为不动杆菌Acinetobactersp.LXK。对该菌的粗酶学特性进行了初步研究,结果表明,最适酶解温度为40℃,酶解最适底物浓度在0.5%,酶解反应体系最适pH在8.0,K+和Ca2+能促进酶解反应,Na+和Mg2+对酶解反应的影响较小,而Fe2+、Mn+和Ba2+对酶解反应起抑制作用。本研究的开展为海洋多糖的深入研究和琼胶寡糖的规模化生产起到了极大的促进作用。
相关新闻推荐
2、肠道微生物及其代谢产物可调节血脑屏障结构和功能完整性(一)
