研究背景
该研究旨在克服由于正选择引起的抗生素结合位点研究的局限性。
研究人员关注大肠杆菌RNA聚合酶(RNAP)中的利福平(Rif)结合位点。
该研究探讨了在Rif结合位点中的单残基突变的遗传图谱,以了解其功能特性。
通过使用多重自动化基因组工程(MAGE),研究人员生成了RNA聚合酶(RNAP)突变体的全面集合。
研究目标
评估Rif结合位点中的突变对Rif结合亲和力和杀菌活性的影响。
研究突变对RNAP速度、核苷酸可用性和细菌对抗生素的敏感性的影响。
分析利福平结合位点的天然序列多样性,以及其与功能性突变和抗生素抗性的关联。
考察转录速度在细菌生理、抗生素抗性和在不同温度下的生长优势中的作用。
研究引起利福平导致的DNA损伤的机制,以及其对细胞存活和DNA修复的影响。
了解转录速度、药物敏感性以及特定药物响应基因的表达之间的关系。
主要发现
研究人员进行了一项研究,以克服由于正选择引起的研究抗生素结合位点的限制。他们在大肠杆菌RNA聚合酶(RNAP)的利福平(Rif)结合位点中生成并分析了760个单残基突变体。
在特定的α螺旋区域中的突变大大影响了利福平的结合,并通过诱导致命性DNA断裂将该药物从细菌生长抑制型转化为杀菌型。
在其他结合位点的突变增加了RNAP速度,导致核苷酸耗尽,细菌更容易受到抗生素的影响,并在较低温度下提供了生长优势。
rpoB基因中的天然序列多样性经常导致功能性利福平结合位点突变,改变了RNAP的特性或赋予了抗药性。
这项研究有助于理解抗生素抗性和必需酶特性。
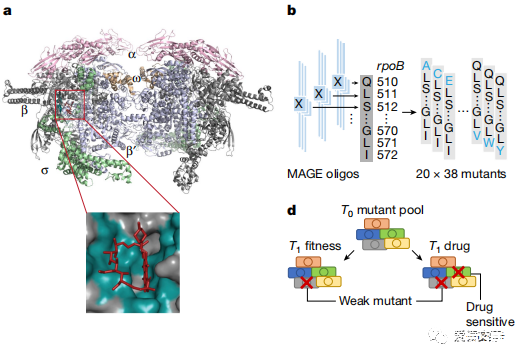
细菌RNA聚合酶的Rif结合位点被明确定义,抗性突变体因突变酶中的变化而表现出不同的表型。
多重自动化基因组工程(MAGE)允许高效而特定地引入和监测突变。
生成了RNA聚合酶(RNAP)突变体的全面集合,以探索利福平(Rif)的结合相互作用以及其杀菌/抑菌效应。
在RNA聚合酶的特定α螺旋区域中的突变改变了利福平的效力,通过诱导DNA断裂将其从抑菌型转化为杀菌型。
增加RNAP速度的突变导致核苷酸耗尽,使细菌更容易受到抗生素的影响,并在较低温度下提供生长优势。
对RNA聚合酶Rif结合位点的突变进行了详细分析,揭示了它们对不同药物的抗性和敏感性的影响。
在特定位置的突变增加了对Rif的抗性,并与特定氨基酸残基在Rif结合中的重要性相关联。
某些突变导致对Rif的高水平抗性,而其他突变则导致对5-氟尿嘧啶(5FU)和双环霉素(BCM)的增加敏感性。
RNAP的速度影响了对5FU和BCM的敏感性或抗性,伴随突变率和核苷酸可用性的改变。
该研究考察了Rif结合位点的天然变异,并确定了具有功能性表型的特定突变。
在特定突变体中观察到对Rif的高水平抗性和增加的敏感性。
在不同细菌物种中流行的特定位置的突变与快速RNAP或特定环境适应性相关。
需要进一步研究以了解这些突变在不同生物体中的影响。
该研究揭示了一种将抑菌型药物转化为杀菌型药物的机制,涉及到增强与其靶标的结合亲和力。
利福平(Rifampicin)诱导双链DNA断裂和SOS反应的激活,导致DNA损伤修复突变体中的细胞死亡。
利福平的作用机制与其他抗生素不同,不依赖于产生活性氧自由基。
提高利福平的结合亲和力可以增强其抗微生物活性并缩短治疗时间。
该研究还确定了影响RNAP速度和对核苷酸耗尽的脆弱性的其他突变。
该研究突出了转录速度在决定核苷酸可用性、改变抗生素敏感性以及改变细菌在不同温度下的最佳生长温度方面的作用。
快速RNAP突变体由于核苷酸耗尽和终止效率低下而导致对某些药物的增加敏感性。
影响RNAP速度的突变体在较低温度下提供了生长优势,但在较高温度下不具备竞争优势。
该研究为细菌生理学、进化和抗生素开发提供了见解和潜在途径。
Rif结合位点显示高度的进化保守性,功能性突变体超越了抗性,为结合位点的“耐药基因组”做出了贡献。
Rif结合位点的多功能性对于旨在增强抗生素效力的药物化学家具有重要意义。
对可变性、抗性和敏感性模式的比较分析可以增进对抗生素机制的理解并指导联合治疗方案的制定。
相关新闻推荐
2、新型广谱阴沟肠杆菌噬菌体ZX14的分离鉴定、生长曲线、体体外杀菌活性实验(三)
